
A lactose, dissacarídeo formado por galactose e glicose, é o principal carboidrato do leite e compõe 6,9% do leite humano e 4,7% do leite bovino.
O leite é um dos principais alimentos para humanos, pois é rico em nutrientes (Tabela 1) que desempenham importante papel na nutrição e desenvolvimento humano ao longo da vida, principalmente durante a infância (Stelwagen, 2022; Vardhanabhuti & Wang, 2022).
O consumo de leite pode ser em sua forma natural ou processado pela indústria de laticínios em produtos lácteos como iogurte e queijo (Didem, Lyne, & Ustunol, 2022). Em 2020, a produção brasileira de leites sob inspeção foi de 25,53 bilhões de litros (EMBRAPA, 2021).
Tabela 1. Composição do leite humano e bovino.
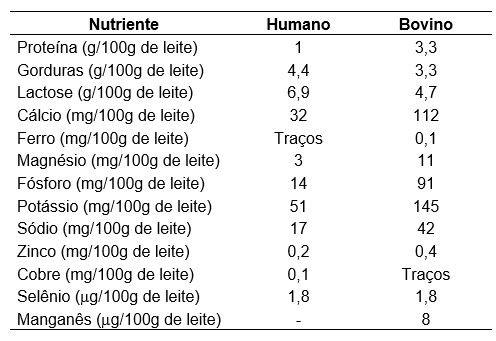
A lactose, dissacarídeo formado por galactose e glicose, é o principal carboidrato do leite e compõe 6,9% do leite humano e 4,7% do leite bovino (Stelwagen; Vardhanabhuti & Wang, 2022). Em mamíferos, a lactose é hidrolisada pela enzima lactase, localizada na superfície apical dos enterócitos na borda em escova do intestino delgado, para ser absorvida (Suri et al., 2019).
A atividade da enzima lactase diminui gradualmente após o desmame, este é um fenômeno natural que resulta na má absorção da lactose. Aproximadamente 70% da população sofre com a absorção inadequada de lactose (Shi, Wu, Xu, & Yu, 2022).
Devido à fermentação da lactose não digerida pela microbiota intestinal, são gerados sintomas de desconforto intestinal como inchaço, gases, cólicas abdominais e diarreia (Vardhanabhuti & Wang, 2022). A quantidade de lactose consumida, o grau de deficiência de lactase e o tipo de produto em que a lactose está contida determinam o grau dos sintomas ocasionados pela má absorção da lactose (Suri et al., 2019).
O tratamento para a intolerância a lactose consiste em restringir completamente o consumo do dissacarídeo permitindo a eliminação dos sintomas associados, além de evitar o desenvolvimento de complicações a longo prazo devido ao quadro de intolerância a lactose não tratada (Suri et al., 2019; Shi et al., 2022).
O leite é considerado uma excelente matéria-prima e os laticínios derivados dele possuem uma densa quantidade de nutrientes e energia (Didem et al., 2022). Desta forma, restringir o consumo de alimentos que possuam lactose não é uma tarefa simples, necessitando monitoramento constante e gerando a sensação de isolamento e pressão social, visto que vários produtos lácteos possuem altas concentrações de lactose (Suri et al., 2019 e Swallow, 2022).
Devido à necessidade dos consumidores, a indústria de alimentos enfrenta o desafio de produzir alimentos seguros, bem aceitos pelo público intolerante a lactose, acessíveis e com aporte nutricional semelhante aos produtos sem restrição de lactose (Suri et al., 2019). No Brasil, alimentos com 100 mg ou menos por 100g ou 100 mL do alimento são considerados isentos de lactose, com mais de 100 mg e menor ou igual a 1 g de lactose em 100 g ou 100 mL são considerados com baixo teor de lactose (ANVISA, 2020).
- O fim de uma atividade produtiva?
- Arco Norte se consolida como rota de entrada e saída de produtos agropecuários
- Marcos Tang é reconduzido à presidência da Gadolando para o biênio 2026-2028
- Conheça o embutido nobre de porco que virou a nova febre da agroindústria, deixando o bacon de lado
- Chinesa dona da maior granja de suínos do mundo prepara entrada no Brasil e mira Mato Grosso e Goiás
O desenvolvimento de produtos sem lactose ocorre com o emprego de enzimas que digerem especificamente este dissacarídeo, fermentação que converte em aditivos alimentares ou filtração por membrana (Hoppe, Byzia, Szymánska, Drozd, & Smiglak; Vardhanabhuti & Wang, 2022).
Atualmente, as enzimas neutras β-galactosidades (EC 3.2.1.23) são amplamente utilizadas para produção de produtos sem lactose, pois em baixas concentrações de lactose (<0,3 mol/L) e alta atividade de água (aW) hidrolisam as ligações β-glicosídicas separando o dissacarídeo em galactose e glicose.
Por outro lado, em altas concentrações de lactose (>0,98 mol/L) e baixa aW a enzima catalisa a formação de ligações β-glicosídicas ao invés de quebrá-las, formando prebiótico galacto-oligossacarídeo (Didem et al., 2022).
As fontes mais comuns de β-galactosidades são fúngicas (Kluyveromyces lactis, Saccharomyces lactis, Kluyveromyces fragilis e Aspergillus oryzae) (Shi et al.; Didem et al.; Hoppe et al., 2022), mas também há fonte bacteriana (como Bifidobacterium bifidum). As β-galactosidades bacterianas são utilizadas principalmente para hidrólise ácida do soro de leite, pois atuam com pH ótimo entre 2,5 e 5,4. Já β-galactosidades fúngicas atuam com pH ótimo entre 6 e 7 indicadas para hidrólise de leite e soro doce (Vardhanabhuti & Wang, 2022).
Na indústria de alimentos, há dois processos utilizados para realizar a hidrólise da lactose: em batelada (pré-hidrólise) e asséptico (pós-hidrolise). Na pré-hidrolise, a enzima é adicionada ao leite cru ou termizado e fica incubada por 24 horas de 4ºC a 8ºC.
Posteriormente, a enzima é inativada por meio do processo térmico de pasteurização ou esterilização para leites UHT (ultra high temperature), não restando atividade enzimática. Neste processo, a dosagem de enzima é relativamente alta, pois é necessária a baixa temperatura e o tempo para a ação das enzimas é limitado, além da incubação do leite necessitar da disponibilidade de um tanque por 24 horas, fatores que podem ser considerados desvantagem para o processo.
Na pós-hidrólise, o leite é tratado termicamente (UHT) antes da adição da enzima e é posteriormente adicionada ao leite para seguir para embalagem. A ação da enzima ocorre à temperatura ambiente durante quarentena de aproximadamente três dias.
Considerando a maior temperatura e tempo de quarentena, o processo de pós-hidrólise utiliza menor concentração de enzimas quando comparado ao processo pré-hidrólise. Para fábricas de alto rendimento o processo pode ser realizado de forma contínua, contudo é necessário equipamentos especiais e operadores altamente qualificados para conduzirem o processo de pós-hidrolise (Dekker, Koenders & Bruins, 2019; Vardhanabhuti & Wang, 2022).
Com a crescente demanda de alimentos sem lactose e com baixo teor de lactose, faz-se necessária a realização de estudos para viabilizar a produção em massa destes alimentos e ofertá-los com menor custo. Contudo, devido ao meio de atuação das enzimas, a estabilidade é um dos fatores que dificultam a utilização de enzimas em grande escala.
O uso de tecnologia rDNA se mostra promissora para o futuro da utilização de enzimas por ofertar material geneticamente modificado que poderia otimizar o processo de hidrólise de lactose em diferentes produtos independentemente das condições de meio, reduzindo o custo de produção. Entretanto, esta possibilidade futura carece de maiores estudos devido à segurança dos alimentos, impacto na saúde humana, fonte de origem e método de produção (Didem et al., 2022).
